截至2023年6月30日,欧洲食品安全局(EFSA)2023年的第二季度批准的新原料数量较第一季度(2023Q1欧盟Novel Food汇总-EFSA批准3个HMO,2个昆虫等10个新原料)显著减少,共计批准4个新原料,其中包括1个HMO——6’SL。瑞旭就具体产品信息整理如下:
表1:获批新原料
|
序号 |
日期 |
名称 |
英文名 |
|
1 |
2023.5.12 |
纤维二糖 |
Cellobiose |
|
2 |
2023.5.15 |
6’-唾液酸乳糖钠盐 |
6’-Sialyllactose sodium salt |
|
3 |
酪蛋白酸铁 |
Ir on milk caseinate | |
|
4 |
2023.5.17 |
卡琪花蒂玛50%乙醇提取物 |
Aqueous ethanolic extract of Labisia pumila |
1. 纤维二糖 (Cellobiose)
2023年5月12日,欧盟委员会发布新条例(EU) 2023/943,根据欧洲议会和理事会法规(EC) No 2015/2283,批准纤维二糖作为新食品投放市场。本法规自2023年6月1日起正式生效。
申报公司: SAVANNA Ingredients GmbH(德国)
自2023年6月1日起的五年内,仅SAVANNA Ingredients GmbH有权在欧盟市场销售纤维二糖,除非:
1. 后续申请人的申报材料符合(EU)2015/2283第26条规定,未参考SAVANNA Ingredients GmbH纳入数据保护的专有科学依据或数据;
2. 后续申请人获得SAVANNA Ingredients GmbH的授权。
批准使用范围和用量见下:
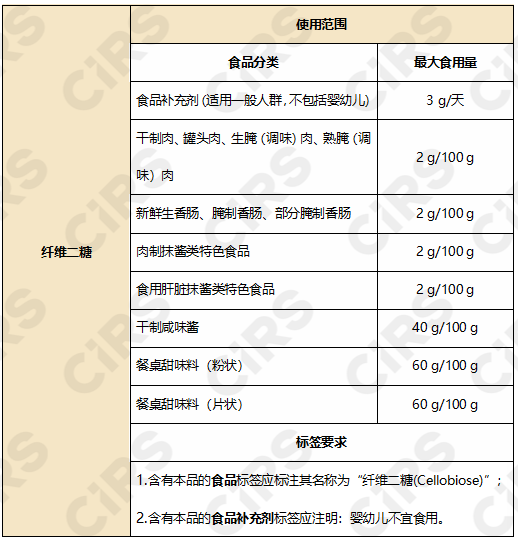
2. 6’-唾液酸乳糖钠盐(微生物来源)6’-Sialyllactose sodium salt produced by derivative strains of E. coli BL21(DE3)
2023年5月15日,欧盟委员会发布新条例(EU) 2023/948,根据欧洲议会和理事会法规(EC) No 2015/2283,批准6’-唾液酸乳糖钠盐(来源:大肠杆菌BL21 (DE3)衍生菌株)作为新食品投放市场。本法规自2023年6月4日起正式生效。
申报公司: 科汉森/Chr. Hansen A/S(丹麦)
自2023年6月4日起的五年内,仅科汉森有权在欧盟市场销售6’-唾液酸乳糖钠盐(来源:大肠杆菌BL21 (DE3)衍生菌株),除非:
1. 后续申请人的申报材料符合(EU)2015/2283第26条规定,未参考科汉森纳入数据保护的专有科学依据或数据;
2. 后续申请人获得科汉森的授权。
批准使用范围和用量见下:
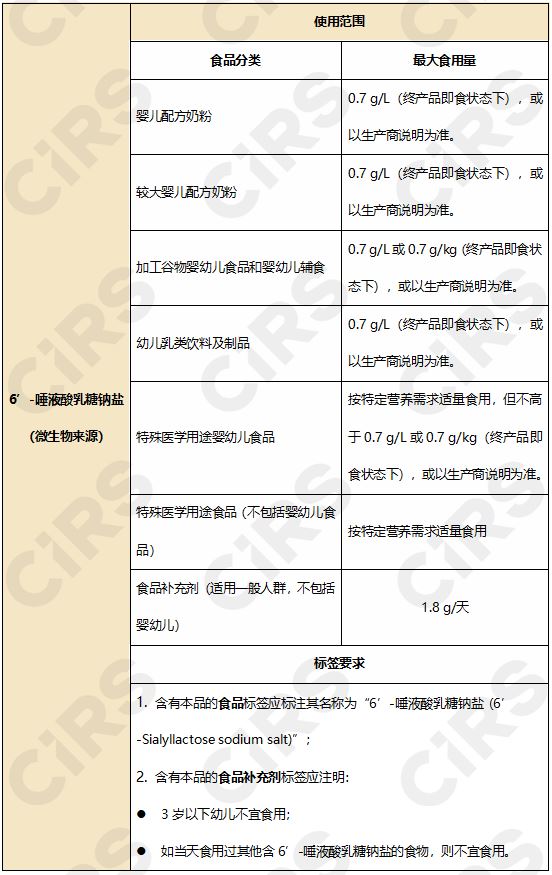
3. 酪蛋白酸铁(Iron milk caseinate )
2023年5月15日,欧盟委员会发布新条例(EU) 2023/949,根据欧洲议会和理事会法规(EC) No 2015/2283,批准酪蛋白酸铁作为新食品投放市场。本法规自2023年6月4日起正式生效。
申报公司: 雀巢/Société des Produits Nestlé S.A.(瑞士)
自2023年6月4日起的五年内,仅雀巢有权在欧盟市场销售酪蛋白酸铁,除非:
1. 后续申请人的申报材料符合(EU)2015/2283第26条规定,未参考雀巢纳入数据保护的专有科学依据或数据;
2. 后续申请人获得雀巢的授权。
批准使用范围和用量见下:
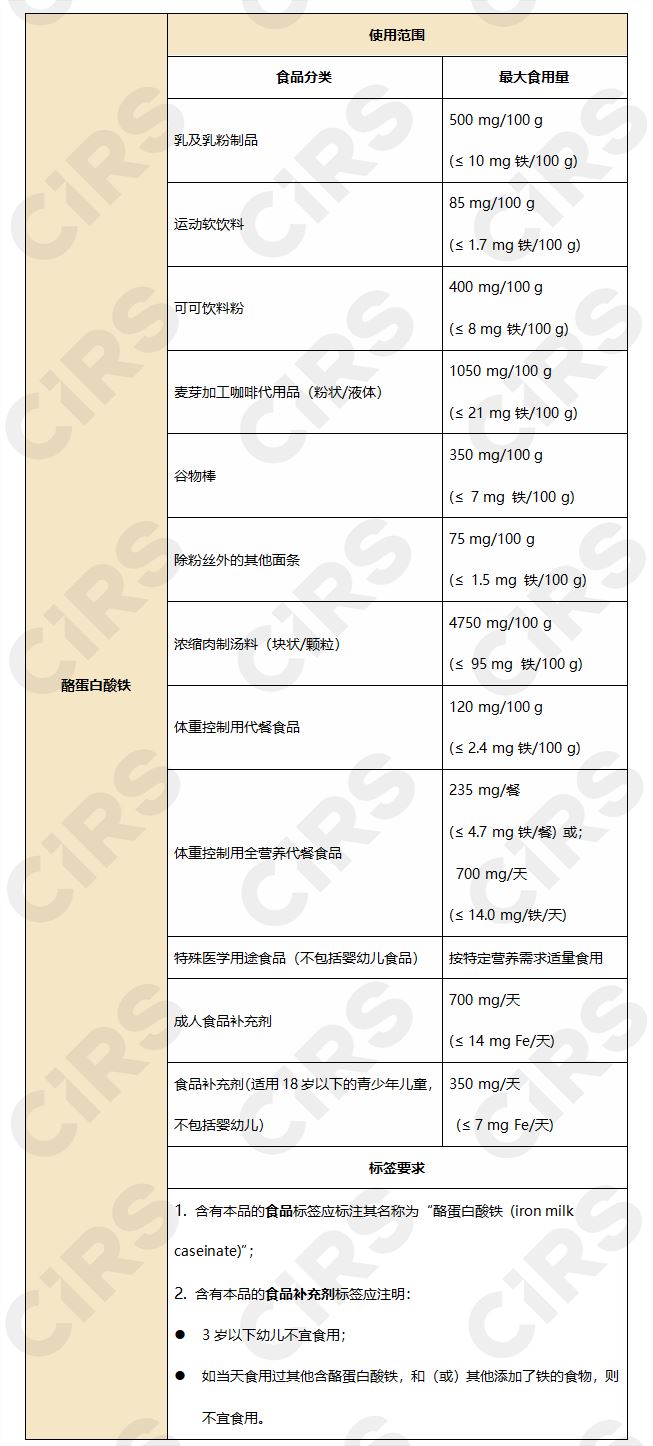
4. 卡琪花蒂玛50%乙醇提取物(Aqueous ethanolic extract of Labisia pumila)
2023年5月17日,欧盟委员会发布新条例(EU) 2023/972,根据欧洲议会和理事会法规(EC) No 2015/2283,批准卡琪花蒂玛50%乙醇提取物作为新食品投放市场。本法规自2023年6月6日起正式生效。
申报公司:Medika Natura Sdn. Bhd.(马来西亚)
自2023年6月6日起的五年内,仅Medika Natura Sdn. Bhd.有权在欧盟市场销售卡琪花蒂玛水醇提取物,除非:
1. 后续申请人的申报材料符合(EU)2015/2283第26条规定,未参考Medika Natura Sdn. Bhd.纳入数据保护的专有科学依据或数据;
2. 后续申请人获得Medika Natura Sdn. Bhd.的授权。
批准使用范围和用量见下:
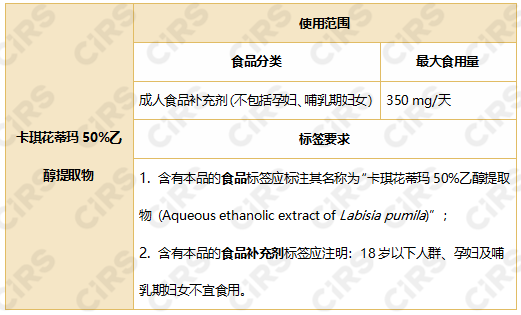
注:文内信息来源于欧盟官方公报(Official Journal of the European Union)。
相关推荐:
