2017年首次进口非特殊化妆品合规流程
1.产品从上海浦东新区口岸进口,且境内责任人注册地在浦东新区
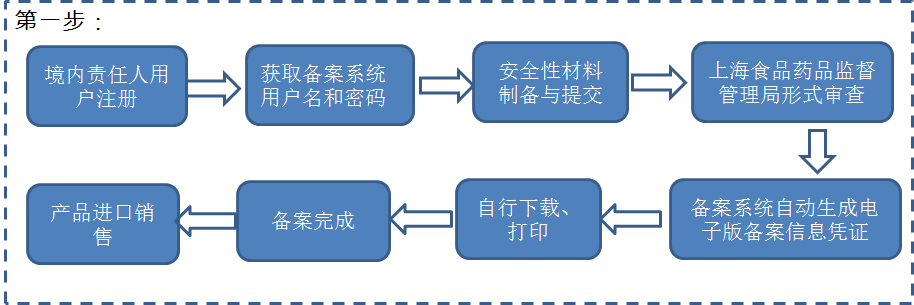
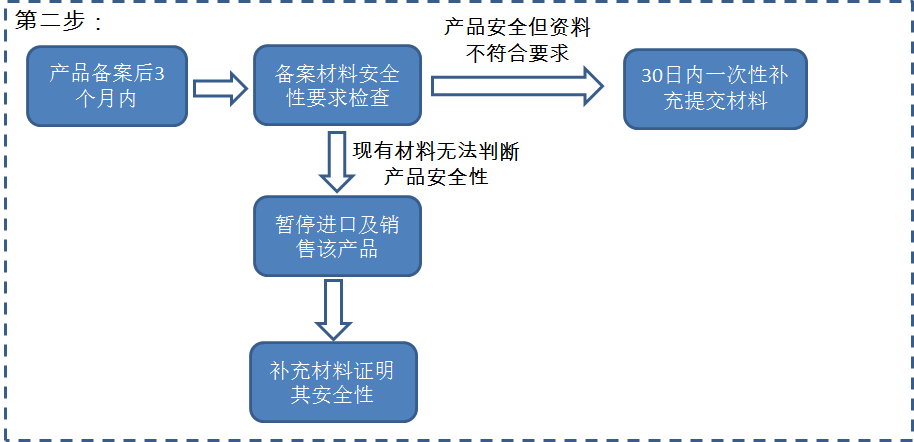
2.产品从上海浦东新区以外口岸进口
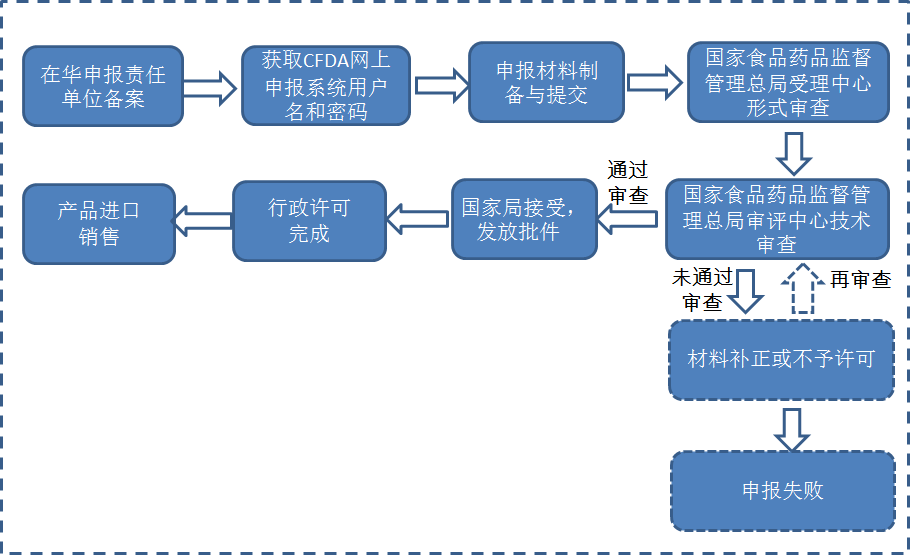
3.不再从上海浦东新区口岸进口的已备案产品
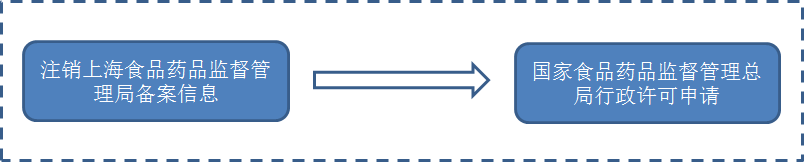
4.产品从上海浦东新区等多个口岸进口
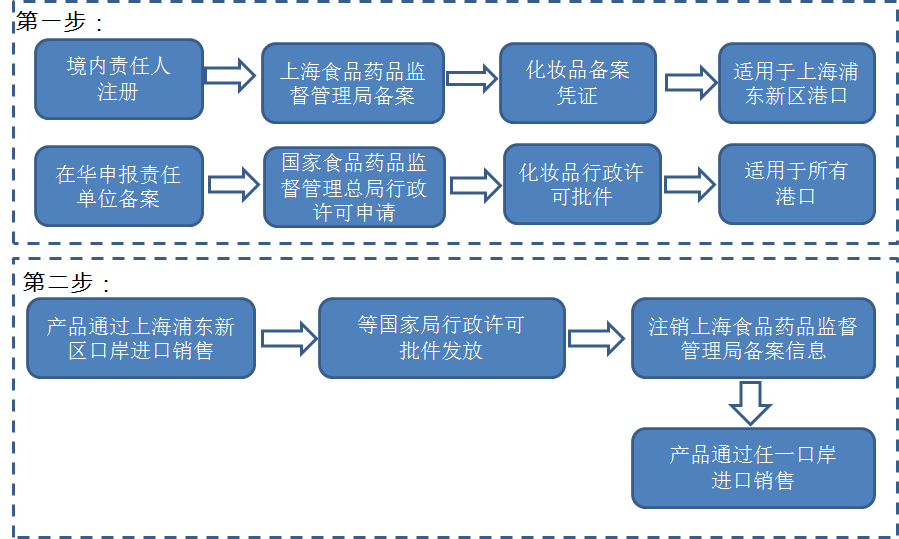
由此看出,2017年企业可以根据实际情况对首次进口非特殊用途化妆品采用不同方式进行市前备案或许可。而特殊用途化妆品仍需要在国家局进行行政审批。以下表格汇总了针对产品类型、进口口岸及企业特点可供企业选择的备案或许可方式。
| 产品类型 | 进口口岸 | 是否在浦东新区注册公司 | 销售模式 | 市前准入方案 |
| 进口非特殊 | 上海浦东新区 | 有 | 线下 | 上海食品药品监督管理局进行备案申请 |
| 进口非特殊 | 上海浦东新区或者多个口岸 | 无 | 线下 | 国家局行政许可申请 |
| 进口非特殊 | 上海浦东新区等多口岸 | 有 | 线下 | 上海食品药品监督管理局备案申请与国家局行政许可申请可同时开展。上海局备案完成后产品可先从浦东新区口岸进口销售。等国家局行政许可申请下来,可注销上海局备案信息,产品仍可在浦东新区及其他任一口岸进口销售 |
| 进口特殊 | - | - | 线下 | 国家局行政许可申请 |
| 国产特殊 | - | - | 线下 | 国家局行政许可申请 |
| 国产非特 | - | - | 线下 | 地方局备案申请 |
| 进口化妆品 | - | - | 线上 | 天津、上海、杭州、宁波、郑州、广州、深圳、重庆、福州、平潭等10个试点城市至2017年12月31日前无需行政许可 |
| 项目 | 国家局行政许可 | 上海局备案 |
| 主管部门 | 国家食品药品监督管理总局 | 上海食品药品监督管理局 |
| 授权申请 | 国外申请人授权在华公司作为在华申报责任单位 | 国外申请人授权在华公司作为境内责任人 |
| 在华公司要求 | 注册地无限制 | 浦东新区注册 |
| 在华公司责任 | 仅负责产品行政许可 | 负责产品进口和经营,并承担产品质量安全责任 |
| 适用范围 | 全国各口岸 | 上海浦东新区 |
| 用户名密码申请 | 国家局行政许可系统 | 上海局备案系统 |
| 用户名密码申请资料 | -申请表 -授权书公证与翻译件 -在华申报责任单位营业执照 |
-申请书 -授权书公证与翻译件 -境内责任人营业执照 |
| 行政许可或备案材料 | (一)申请表; (二)产品中文名称命名依据; (三)产品配方; (四)产品质量安全控制要求; (五)产品原包装; (六)经卫生部认定的检验机构出具的检验报告及相关资料; (七)产品中可能存在安全性风险物质的有关安全性评估资料; (八)已经备案的行政许可在华申报责任单位授权书复印件及营业执照复印件并加该公章; (九)化妆品使用原料及原料来源符合疯牛病区高风险物质禁限用要求的承诺书; (十)自由销售证明; (十一)可能有助于评审的其它资料; (十二)生产工艺简述和简图; (十三)化妆品产品技术要求的文字版资料。 提供原件1份,另附未启封的市售样品1件。 |
(一)申请表; (二)产品中文名称命名依据; (三)产品配方; (四)产品质量安全控制要求; (五)产品原包装图片; (六)产品生产工艺简述; (七)产品技术要求; (八)化妆品行政许可检验机构出具的检验报告及相关资料; (九)产品中可能存在安全性风险物质的有关安全性评估资料; (十)化妆品适用原料及原料来源符合疯牛病疫区高风险物质禁限用要求的承诺书; (十一)自由销售证明; (十二)境外生产企业生产质量管理的相关证明材料; (十三)参照《化妆品行政许可申报受理规定》(国食药监许〔2009〕856号,以下称《申报受理规定》)要求,可能有助于备案的其他资料 |
| 资料形式审查机构 | 国家局行政受理中心 | 上海食品药品监督管理局 |
| 技术审查 | 形式审查后移交总局保健食品审评中心进行技术审查 | 产品备案后3个月内开展 |
| 许可或者备案凭证 生成流程及形式 |
技术审查通过后发放行政许可批件证书 | 形式审查通过后备案系统自动生成电子版备案信息凭证供企业自行下载打印 |
| 批准或备案凭证编号格式 | 国妆备进字J+四位年份数字+四位编号 | 国妆网备进字(沪)+四位年份数字+六位顺序编号 |
| 批准或备案凭证 有效期 |
4年 | 未知 |
| 已批准或备案产品 不再进口 |
无要求 | 境内责任人注销备案信息 |
由上表看出,国家局行政许可与上海局备案模式最大的差异体现在许可或备案流程及境内责任人的要求。上海局备案最大优势体现在企业通过资料形式审查后就可以获得备案号进行进口销售。国家局行政许可要求在通过所有形式和技术审查后才能获得许可号进行进口销售。两者相比,前者更利于企业将产品快速投放市场。更多加强市后监管。但在资料要求上,两者几乎保持一致。虽然新的备案工作程序要求已经发布,但在实际操作中无论企业还是主管部门仍然将面临很多未知的问题。至少从法规层面看出政府希望保持相同技术审评尺度,只是调整许可程序和监管方式。除此之外,新的备案方式对境内责任人的要求较高。需要境内责任人承担产品的进口和经营,并同时承担产品的质量安全责任。而传统许可方式的在华申报责任单位仅限于对产品申报相关事项承担责任。由此看出,境内企业在选择新的备案方式前需谨慎考虑产品上市后的质量安全风险。总之,由上海浦东新区试点实施首次进口非特殊用途化妆品备案模式看出,政府已经对2016年第24号文件及2015年食品药品监管总局关于对取消和下放行政审批事项加强事中事后监管的意见作出响应和落实。
