2023年11月8日、11月9日,国家市场监督管理总局食品审评中心分别就保健食品的2个常见问题和2个共性问题进行了解答,详情见下。
常见问题:
1.《允许保健食品声称的保健功能目录 非营养素补充剂(2023年版)》发布后,申报材料的申请表中的保健功能应如何填写?
答: 新产品申请表中保健功能一项应按新的功能目录填写;变更、延续、转让、补发申请表中保健功能应与获批证书中载明内容保持一致。
2. 保健食品纸质版受理通知书依然需要领取吗?
答: 目前保健食品注册管理信息系统系统升级,申报端可以领取电子版的受理通知书。故现场递交申报材料的可不再领取纸质版受理通知书;邮寄申报材料的,受理大厅也不再邮寄纸质版受理通知书。
如有特殊情况,需要领取或邮寄的,请在申报材料随附说明。
共性问题:
1. 对于保健食品功能论证报告中功能声称科学依据的要求?
答: 科学依据及其相关综述内容应当完整规范,不仅包括科学依据的来源、目录和全文,还应当与产品的配方、工艺等技术要求进行研究比对,对产品配方及其功能声称科学依据充足性进行论证和综述。文献依据包括在国内核心专业期刊或国际专业期刊正式发表的科研论文;我国传统本草典籍的有关记述;文献分析和评价报告;国际公认的食品卫生权威机构、组织,或我国有关部门、权威机构正式发布的国际标准、国家标准、风险评估报告、统计信息等,汇总信息应完整准确,能够对产品配方及其功能声称形成有效支撑。报纸、网评、非科研杂志、专利文书、产品宣传页等不属于国内核心专业期刊等资料,视为无效资料,不纳入审评范围。
鼓励申请人对产品配方主要原料的功能依据及其他原料的配伍必要性相关文献依据,进行全面系统的检索和筛选,通过Meta分析等方法进行文献系统分析,提出对产品保健功能科学依据充足性和配方合理性的文献分析和评价报告。
2. 对于保健食品功能论证报告中引用文献汇总表的要求?
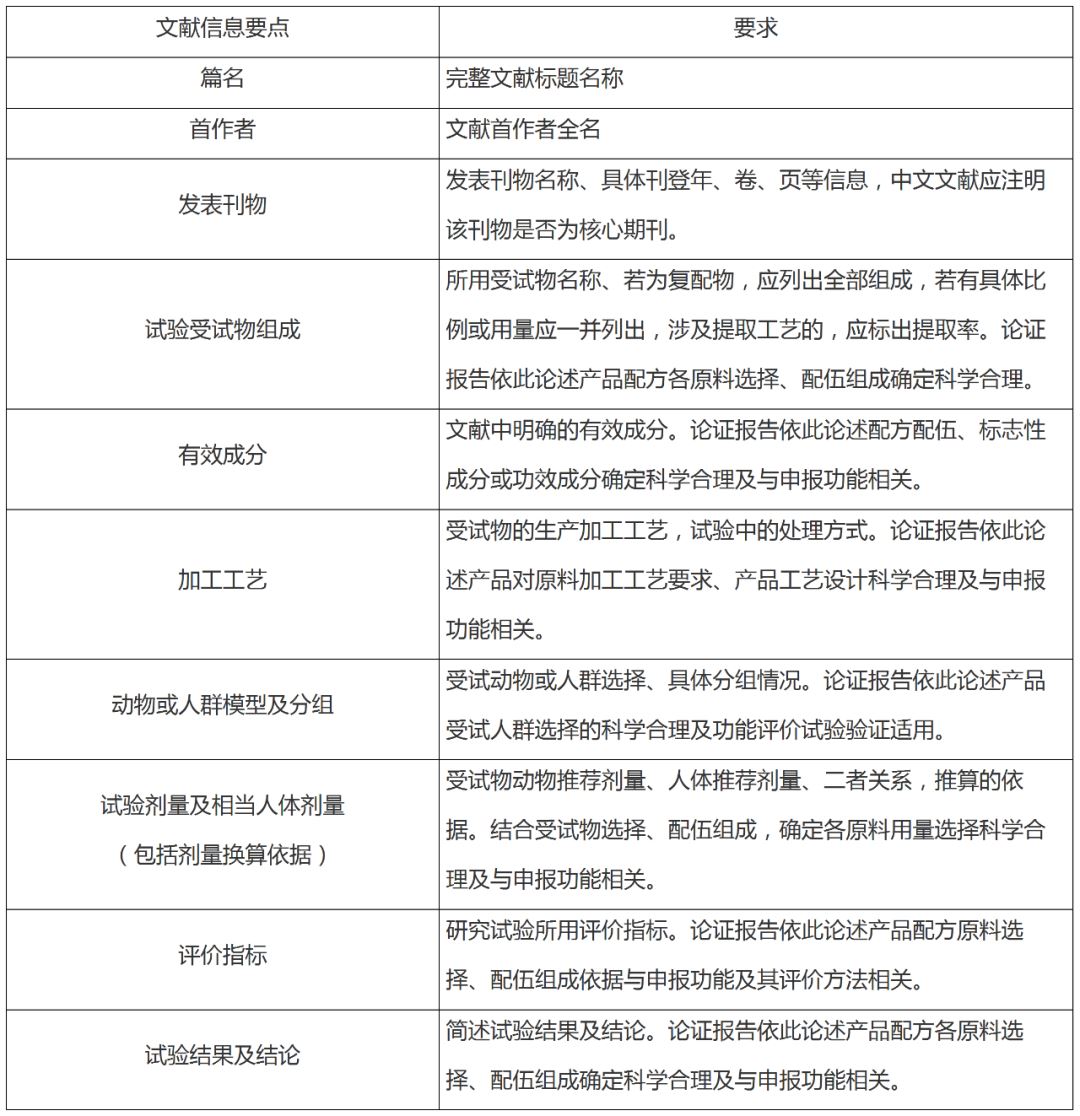
答: 应包括篇名、首作者、发表刊物及是否为核心期刊、试验受试物组成、主要成分、加工工艺,动物或人群模型及分组、试验剂量及相当人体剂量(包括剂量换算依据)、评价指标,试验结果及结论等信息。要求见下表: